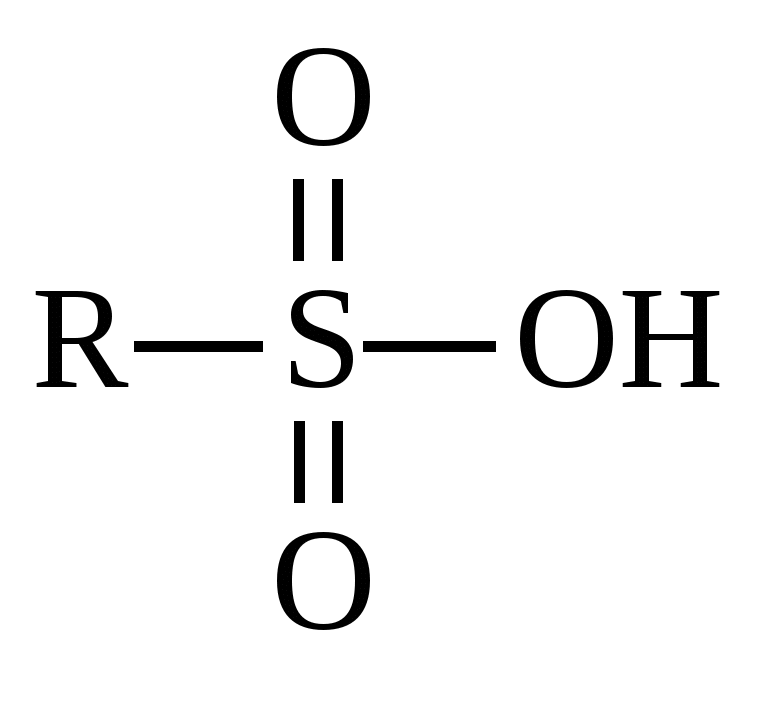Конспект занятия "Теория строения органических соединений."
Классификация органических соединений по природе функциональной группы и по строению углеродного скелета
Органические соединения наиболее часто классифицируются по двум критериям - по строению углеродного скелета молекулы или по наличию в молекуле органического соединения функциональной группы.
Классификацию органических молекул по строению углеродного скелета можно представить в виде схемы:
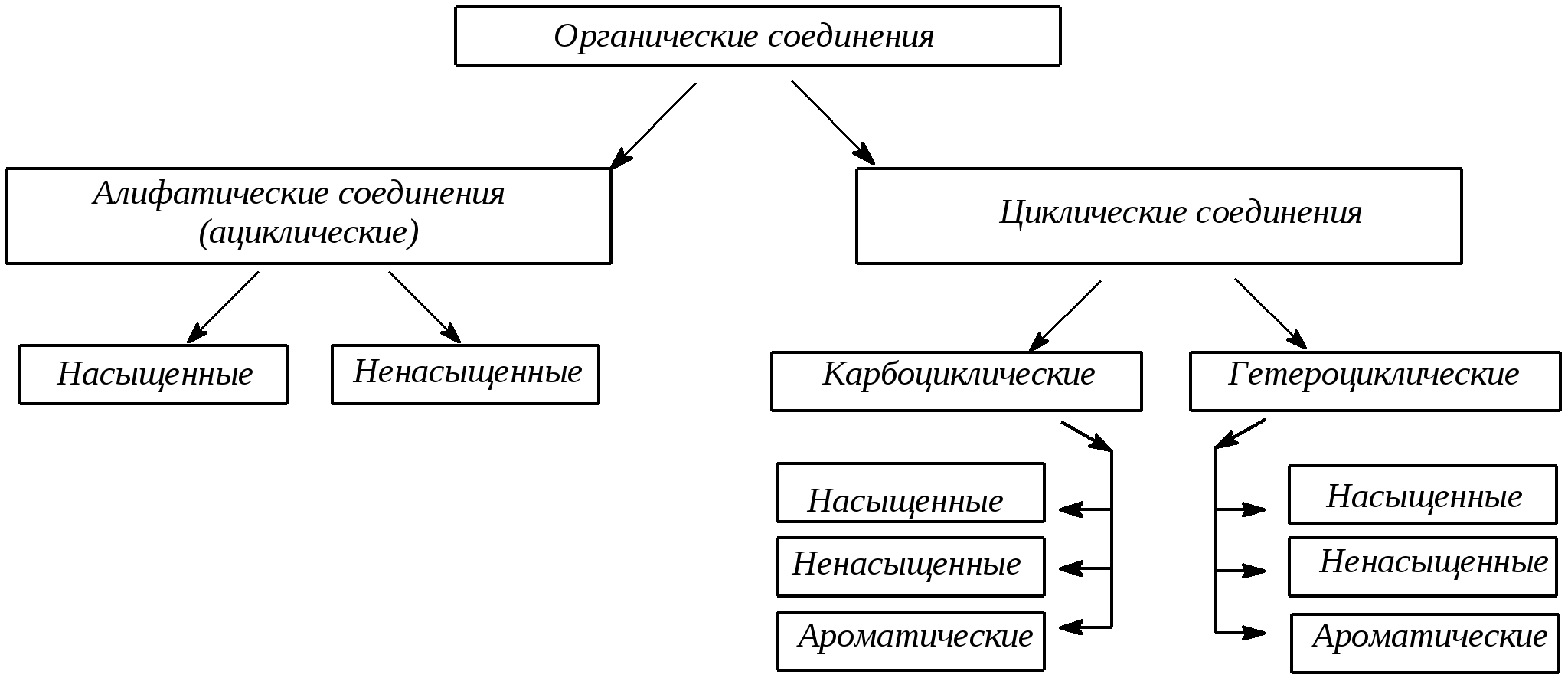
Ациклические соединения – это соединения с незамкнутой углеродной цепью. Их основу составляют алифатические соединения (от греческого aleiphatos – масло, жир, смола) – углеводороды и их производные, углеродные атомы которых связаны между собой в открытые неразветвленные или разветвленные цепи.
Циклические соединения – это соединения, содержащие замкнутую цепь. Карбоциклические соединения в составе цикла содержат только атомы углерода, гетероциклические в составе цикла, кроме атомов углерода, содержат один или несколько гетероатомов (атомы N,O,Sи др.).
В зависимости от природы функциональной группы производные углеводородов делят на классы органических соединений. Функциональная группа– это атом или группа атомов, как правило, неуглеводородного характера, которые определяют типичные химические свойства соединения и его принадлежность к определенному классу органических соединений. В качестве функциональной группы у ненасыщенных молекул выступают двойные или тройные связи.
| Название функциональной группы | Название класса соединений | Общая формула класса |
| Карбоксильная -COOH | Карбоновые кислоты | 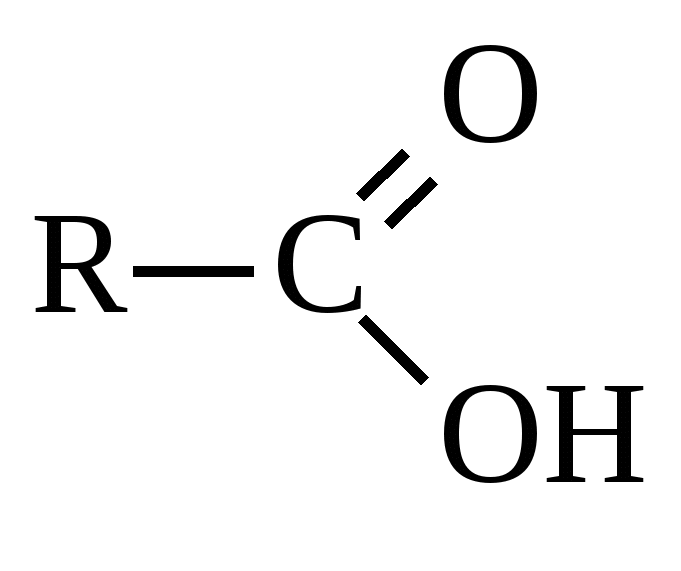
|
| Сульфоновая -SO3H | Сульфокислоты | 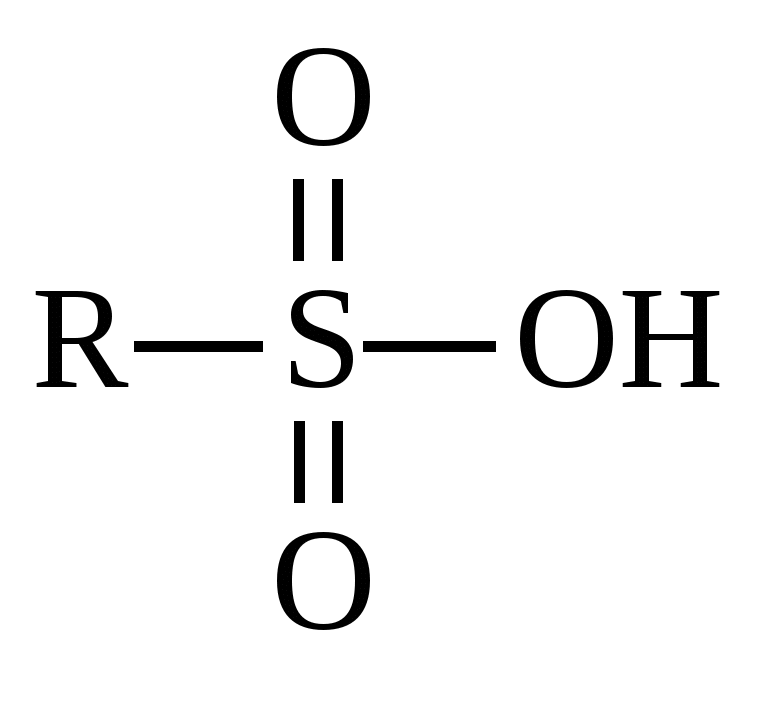
|
| Циано -CN | Нитрилы | NR-C |
| Оксогруппа (карбонильная) 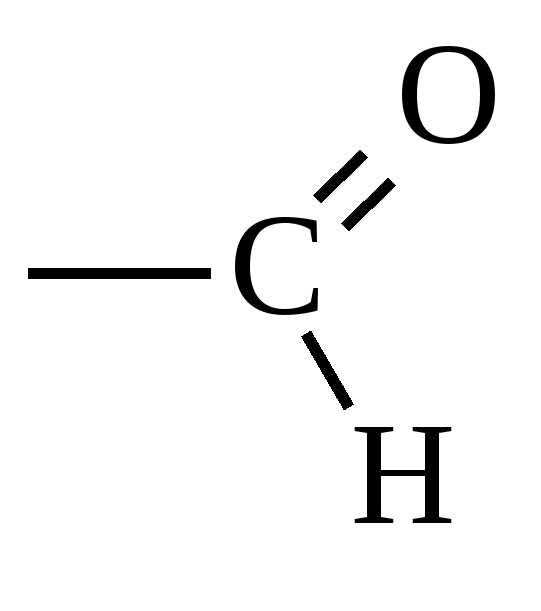
| Альдегиды | 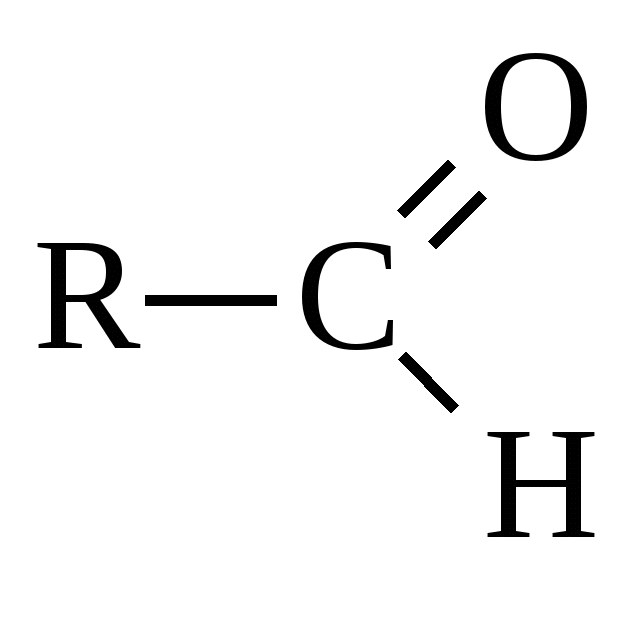
|
| Оксогруппа (карбонильная) 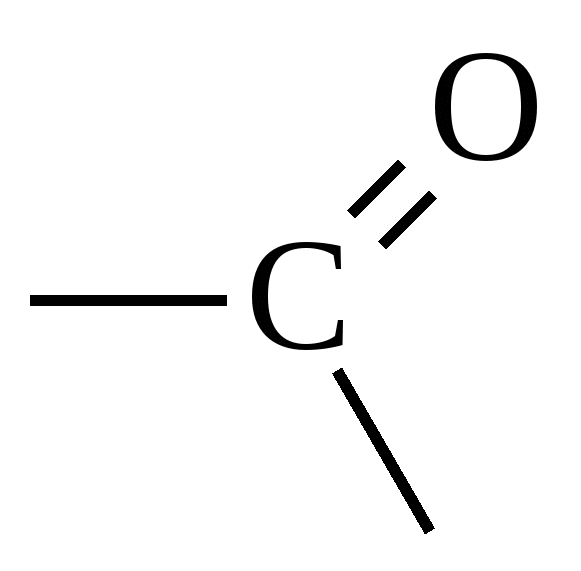
| Кетоны | 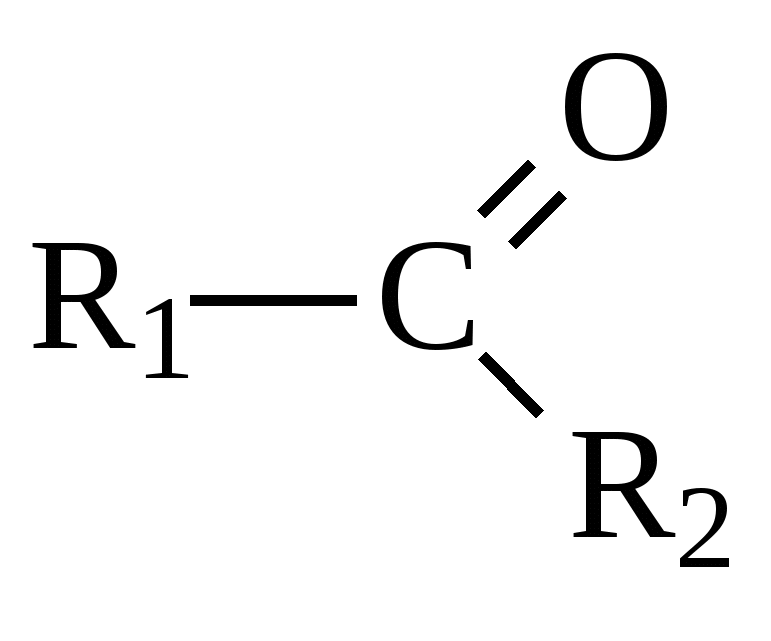
|
| Гидроксильная -OH | Спирты | R-O-H |
| Тиольная (меркапто) -SH | Тиолы (меркаптаны) | R-S-H |
| -F, -Cl, -Br, -I | Галогенпроизводные | R-Hal |
| Алкоксильная - OR | Простые эфиры | R-O-R |
| Алкилтиольная -SR | Тиоэфиры | R-S-R |
| -NO2 | Нитросоединения | R-NO2 |
| Алкосикарбонильная 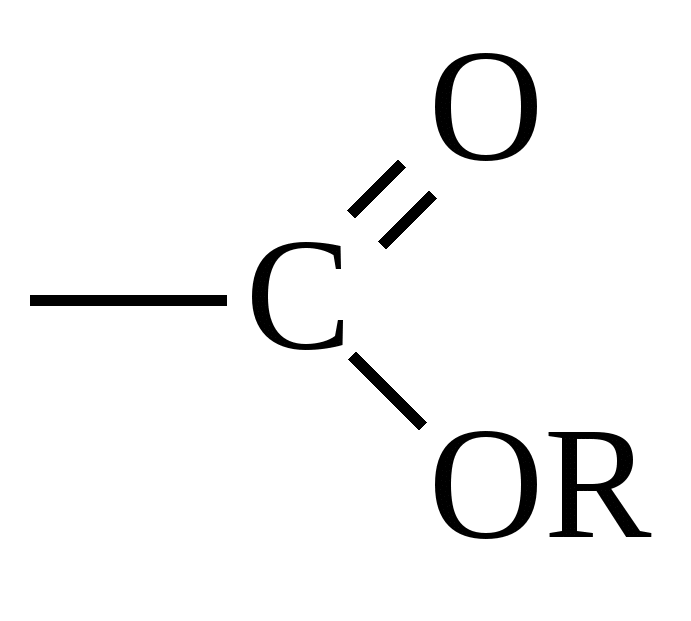
| Сложные эфиры | 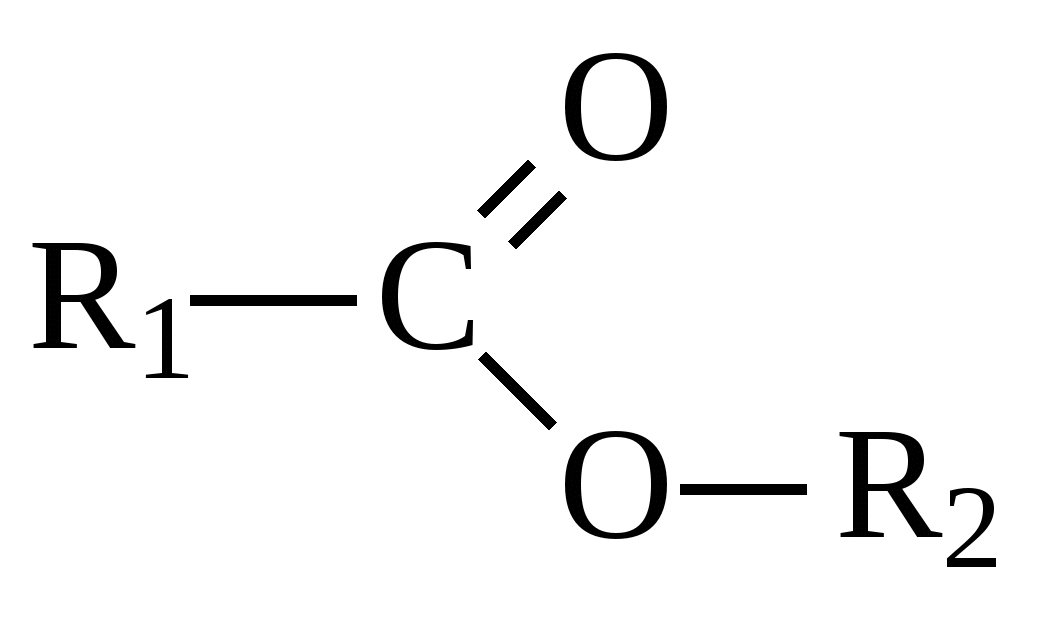
|
| Амино -NH2 | Амины | RNH2,R1NHR2,R1R2R3N |
| Карбоксамидная 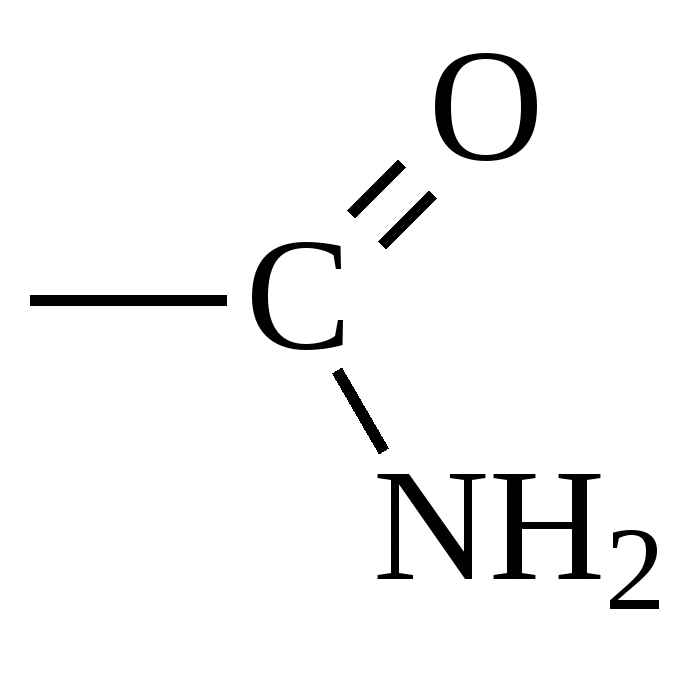
| Амиды | 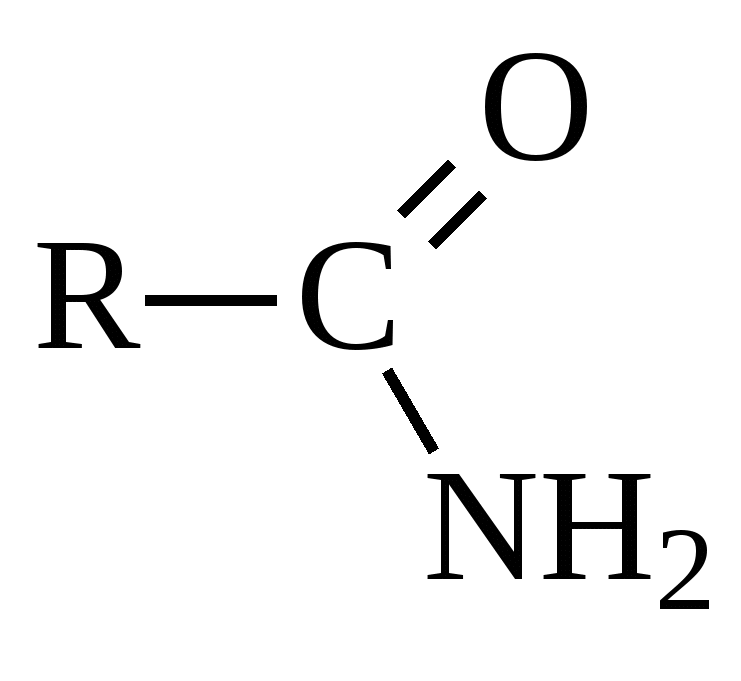
|
Гомологический ряд – ряд соединений, близких по свойствам и отличающихся по составу на одну или несколько групп СН2.
Члены гомологического ряда называются гомологами.
Гомологи – соединения, близкие по свойствам, и отличающиеся по составу на одну или несколько групп СН2.
Понятие «гомологический ряд» является очень важным в органической химии. Гомологические ряды существуют для всех классов органических соединений. В гомологические ряды объединяют соединения, проявляющие сходные свойства, но имеющие разную длину углеводородной цепи. Например, представители класса спиртов метиловый и этиловый спирты. Структурные формулы этих веществ СН3–ОН и С2Н5–ОН. Состав их различается на группу СН2. Важнейшие химические свойства этих соединений определяются не длиной углеводородной цепи молекулы, а наличием в ней гидроксильной группы. Учитывая огромное множество органических соединений, изучать их по отдельности, как в неорганической химии, не представляется возможным, поэтому сходные по свойствам вещества объединяют в гомологические ряды и изучают свойства, присущие всем гомологам.

Изомерия – явление, заключающееся в существовании соединений, имеющих одинаковый качественный и количественный состав, но разное строение молекул.
Рассмотрим явление изомерии на примере углеводорода, молекулы которого содержат пять атомов углерода. Этот углеводород называется пентан. Молекулярная формула его С5Н12. Пентан имеет три изомера, структурные формулы которых следующие:
СН3
![]()
СН3–СН2–СН2–СН2–СН3 СН3–СН–СН2–СН3 СН3–С–СН3
![]()
![]()
СН3 СН3
Очевидно, что для углеводородов с бóльшим числом атомов углерода в молекуле число изомеров будет весьма значительным. Так, например, углеводородов состава С20Н42 насчитывается 336319, а для С40Н82 число возможных изомеров оценивается в астрономическую величину порядка 1012!
Явление изомерии во многом обусловливает многообразие органических соединений, делает органическую химию поистине неисчерпаемой.