Металлы первой А группы (Щелочные металлы)
— это элементы 1-й группы периодической таблицы химических элементов (по устаревшей классификации — элементы главной подгруппы I группы): литий Li, натрий Na, калий K, рубидий Rb, цезий Cs, франций Fr. При растворении щелочных металлов в воде образуются растворимые гидроксиды, называемые щёлочами.
| Содержание 1 Общая характеристика щелочных металлов 2 Химические свойства щелочных металлов 3 Получение щелочных металлов 4 Соединения щелочных металлов 4.1 Гидроксиды 4.2 Карбонаты 5 Фотографии 6 Литература 7 Примечания 8 См. также 9 Ссылки |
Общая характеристика щелочных металлов
В Периодической системе они следуют сразу за инертными газами, поэтому особенность строения атомов щелочных металлов заключается в том, что они содержат один электрон на внешнем энергетическом уровне. Очевидно, что валентные электроны щелочных металлов могут быть легко удалены, потому что атому энергетически выгодно отдать электрон и приобрести конфигурацию инертного газа. Поэтому для всех щелочных металлов характерны восстановительные свойства. Это подтверждают низкие значения их потенциалов ионизации (потенциал ионизации атома цезия — один из самых низких) и электроотрицательности (ЭО).



Литий Натрий Калий



Рубидий Цезий Франций
Некоторые атомные и физические свойства щелочных металлов
| Атомный
номер | Название,
символ | Число природных изотопов | Атомная масса | Металл. радиус, нм | tпл,
°C | tкип,
°C | ρ,
г/см³ |
| 3 | Литий Li | 2 | 6,941(2) | 0,152 | 180,6 | 1342 | 0,534 |
| 11 | Натрий Na | 1 | 22,989768(6) | 0,186 | 97,8 | 883 | 0,968 |
| 19 | Калий К | 2+1а | 39,0983(1) | 0,227 | 63,07 | 759 | 0,856 |
| 37 | Рубидий Rb | 1+1а | 85,4687(3) | 0,248 | 39,5 | 688 | 1,532 |
| 55 | Цезий Cs | 1 | 132,90543(5) | 0,265 | 28,4 | 671 | 1,90 |
| 87 | Франций Fr | 1а | (223) | — | 20 | 690 | 1,87 |
Все металлы этой подгруппы имеют серебристо-белый цвет (кроме серебристо-жёлтого цезия), они очень мягкие, их можно резать скальпелем. Литий, натрий и калий легче воды и плавают на её поверхности, реагируя с ней.
Щелочные металлы встречаются в природе в форме соединений, содержащих однозарядные катионы. Многие минералы содержат в своём составе металлы главной подгруппы I группы.
Химические свойства щелочных металлов
Из-за высокой химической активности щелочных металлов по отношению к воде, кислороду, и иногда даже и азоту (Li, Cs) их хранят под слоем керосина. 
1. Взаимодействие с водой. Важное свойство щелочных металлов — их высокая активность по отношению к воде. Наиболее спокойно (без взрыва) реагирует с водой литий:

При проведении аналогичной реакции натрий горит жёлтым пламенем и происходит небольшой взрыв. Калий ещё более активен: в этом случае взрыв гораздо сильнее, а пламя окрашено в фиолетовый цвет.
2. Взаимодействие с кислородом. Продукты горения щелочных металлов на воздухе имеют разный состав в зависимости от активности металла.

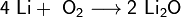
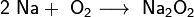
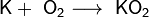
Для получения оксидов натрия и калия нагревают смеси гидроксида с избытком металла в отсутствие кислорода:

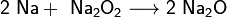
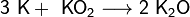
| Формула
кислородного соединения | Цвет |
| Li2O | Белый |
| Na2O | Белый |
| K2O | Желтоватый |
| Rb2O | Жёлтый |
| Cs2O | Оранжевый |
Оксиды щелочных металлов обладают всеми свойствами, присущими основным оксидам: они реагируют с водой, кислотными оксидами и кислотами:
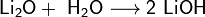
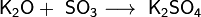
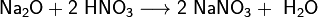
3. Взаимодействие с другими веществами. Щелочные металлы реагируют со многими неметаллами. При нагревании они соединяются с водородом с образованием гидридов, с галогенами, серой, азотом, фосфором, углеродом и кремнием с образованием, соответственно, галогенидов, сульфидов, нитридов, фосфидов, карбидов и силицидов:
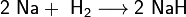
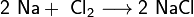
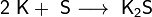
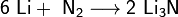
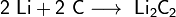
Щелочные металлы взаимодействуют с органическими веществами спиртами (с образованием алкоголятов) и карбоновыми кислотами (с образованием солей):


4. Качественное определение щелочных металлов. Поскольку потенциалы ионизации щелочных металлов невелики, то при нагревании металла или его соединений в пламени атом ионизируется, окрашивая пламя в определённый цвет:
Окраска пламени щелочными металлами
и их соединениями
| Щелочной металл | Цвет пламени |
| Li | Карминно-красный |
| Na | Жёлтый |
| K | Фиолетовый |
| Rb | Бурокрасный |
| Cs | Фиолетово-красный |

Получение щелочных металлов
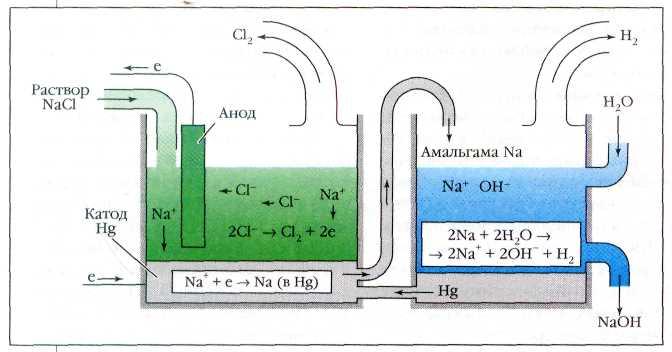
1. Для получения щелочных металлов используют в основном электролиз расплавов их галогенидов, чаще всего — хлоридов, образующих природные минералы:
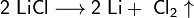
2. Иногда для получения щелочных металлов проводят электролиз расплавов их гидроксидов:
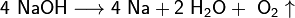
3. Щелочной металл может быть восстановлен из соответствующего хлорида или бромида кальцием, магнием, кремнием и др. восстановителями при нагревании под вакуумом до 600-900 °C:

Соединения щелочных металлов
Гидроксиды
Для получения гидроксидов щелочных металлов в основном используют электролитические методы. Наиболее крупнотоннажным является производство гидроксида натрия электролизом концентрированного водного раствора поваренной соли:

Прежде щёлочь получали реакцией обмена:

Получаемая таким способом щёлочь была сильно загрязнена содой Na2CO3.
Карбонаты
Важным продуктом, содержащим щелочной металл, является сода Na2CO3. Основное количество соды во всём мире производят по методу Сольве, предложенному ещё в начале XX века. Суть метода состоит в следующем: водный раствор NaCl, к которому добавлен аммиак, насыщают углекислым газом при температуре 26 — 30 °C. При этом образуется малорастворимый гидрокарбонат натрия, называемый питьевой содой:
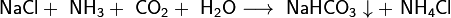
В отличие от малорастворимой кислой соли NaHCO3, гидрокарбонат калия KHCO3 хорошо растворим в воде, поэтому карбонат калия, или поташ, K2CO3 получают действием углекислого газа на раствор гидроксида калия:
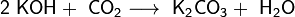
Поташ используют в производстве стекла и жидкого мыла.
Металлы второй А группы (щёлочноземельные металлы)
Металлы названы так потому, что их оксиды сообщают в воде щелочную реакцию. Кроме того, оксиды по тугоплавкости сходны с оксидами алюминия и железа, носившими ранее общее название «земли».
В более строгом понимании к щёлочноземельным металлам относят только кальций, стронций, барий и радий, реже магний . Первый элемент этой подгруппы, бериллий, по большинству свойств гораздо ближе к алюминию, чем к высшим аналогам группы, в которую он входит. Второй элемент этой группы, магний, также в некоторых отношениях значительно отличается от щёлочноземельных металлов в указанном выше значении этого термина.



Бериллий Be Магний Mg Кальций Ca



Стронций Sr Барий Ba Барий Ba
Некоторые атомные и физические свойства щелочноземельных металлов
| Атомный
номер | Название,
символ | Число природных изотопов | Атомная масса | Металл.радиус, нм | tпл,
°C | tкип,
°C | ρ,
г/см³ |
| 4 | Бериллий Be | 1+11а | 9,012182 | 0,169 | 1278 | 2970 | 1,848 |
| 12 | Магний Mg | 3+19а | 24,305 | 0,24513 | 650 | 1105 | 1,737 |
| 20 | Кальций Ca | 5+19а | 40,078 | 0,279 | 839 | 1484 | 1,55 |
| 38 | Стронций Sr | 4+35а | 87,62 | 0,304 | 769 | 1384 | 2,54 |
Физические свойства
Все щёлочноземельные металлы — серые, твёрдые при комнатной температуре вещества. В отличие от щелочных металлов, они существенно более твёрдые, и ножом преимущественно не режутся (исключение — стронций). Плотность щёлочноземельных металлов с порядковым номером растёт, хотя явно рост наблюдается только начиная с кальция. Самый тяжёлый — радий, по плотности сравнимый с железом (ρ= 7,874 г/см3).

Химические свойства
Щёлочноземельные металлы имеют электронную конфигурацию внешнего энергетического уровня ns², и являются s-элементами, наряду с щелочными металлами. Имея два валентных электрона, щёлочноземельные металлы легко их отдают, и во всех соединениях имеют степень окисления +2 (очень редко +1).

Химическая активность щёлочноземельных металлов растёт с ростом порядкового номера. Магний защищён оксидной плёнкой при комнатной температуре и более высоких (до 650 °C) температурах и не окисляется дальше. Кальций медленно окисляется и при комнатной температуре вглубь (в присутствии водяных паров), и сгорает при небольшом нагревании в кислороде, но устойчив в сухом воздухе при комнатной температуре. Стронций, барий и радий быстро окисляются на воздухе, давая смесь оксидов и нитридов, поэтому их, так же и как щелочные металлы (и кальций), хранят под слоем керосина.
Простые вещества
Бериллий реагирует со слабыми и сильными растворами кислот с образованием солей:

Реакция бериллия с водными растворами щелочей сопровождается выделением водорода и образованием гидроксобериллатов:

Магний, кальций, стронций, барий и радий реагируют с водой с образованием щелочей (кроме магния, реакция которого с водой происходит только при внесении раскалённого порошка магния в воду, и кальция, гидроксид которого плохо растворим в воде, и, следственно, не может быть назван щелочью):
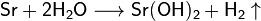
Оксиды

Оксид бериллия - амфотерный оксид, растворяется в концентрированных минеральных кислотах и щелочах с образованием солей:
но с менее сильными кислотами и основаниями реакция уже не идет.
Оксид магния не реагирует с разбавленными и концентрированными основаниями, но легко реагирует с кислотами и водой:
Оксиды кальция, стронция, бария и радия - основные оксиды, реагируют с водой, сильными и слабыми растворами кислот и амфотерными оксидами и гидроксидами:
Гидроксиды
Гидроксид бериллия амфотерен, при реакциях с сильными основаниями образует бериллаты, с кислотами - бериллиевые соли кислот:
Гидроксиды магния, кальция, стронция, бария и радия - основания, сила увеличивается от
слабого до очень сильного , являющегося сильнейшим коррозионным веществом, по активности превышающим гидроксид калия. Хорошо растворяются в воде (кроме гидроксидов магния и кальция). Для них характерны реакции с кислотами и кислотными оксидами и с амфотерными оксидами и гидроксидами:
Нахождение в природе
Все щёлочноземельные металлы имеются (в разных количествах) в природе. Ввиду своей высокой химической активности все они в свободном состоянии не встречаются. Самым распространённым щёлочноземельным металлом является кальций, количество которого равно 3,38 % (от массы земной коры). Немногим ему уступает магний, количество которого равно 2,35 % (от массы земной коры). Распространены в природе также барий и стронций, которых соответственно 0,05 и 0,034 % от массы земной коры. Бериллий является редким элементом, количество которого составляет 6·10−4% от массы земной коры. Что касается радия, который радиоактивен, то это самый редкий из всех щёлочноземельных металлов, но он в небольшом количестве всегда содержится в урановых рудах. В частности, он может быть выделен оттуда химическим путём. Его содержание равно 1·10−10% (от массы земной коры)[5].
Биологическая роль
Магний содержится в тканях животных и растений (хлорофилл), является кофактором многих ферметативных реакций, необходим при синтезе АТФ, участвует в передаче нервных импульсов, активно применяется в медицине (бишофитотерапия и др.). Кальций — распространенный макроэлемент в организме растений, животных и человека. В организме человека и других позвоночных большая его часть находится в скелете и зубах. В костях кальций содержится в виде гидроксиапатита. Из различных форм карбоната кальция (извести) состоят "скелеты" большинства групп беспозвоночных (губки, коралловые полипы, моллюски и др.). Ионы кальция участвуют в процессах свертывания крови, а также служат одним из универсальных вторичных посредников внутри клеток и регулируют самые разные внутриклеточные процессы — мышечное сокращение, экзоцитоз, в том числе секрецию гормонов инейромедиаторов. Стронций может замещать кальций в природных тканях, т.к. схож с ним по свойствам. В организме человека масса стронция составляет около 1% от массы кальция.