АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ (АРЕНЫ)
Ароматические соединения — циклические органические соединения, которые имеют в своём составе ароматическую систему. Основными отличительными свойствами являются повышенная устойчивость ароматической системы и, несмотря на ненасыщенность, склонность к реакциям замещения, а не присоединения.
Типичными представителями ароматических углеводородов являются производные бензола, т.е. такие карбоциклические соединения, в молекулах которых имеется особая циклическая группировка из шести атомов углерода, называемая бензольным или ароматическим ядром.
Общая формула ароматических углеводородов CnH2n-6.
Углеводороды ароматические получили свое название оттого, что очень часто их производные обладают приятным запахом и встречаются в различных смолах, эфирных маслах и пр. Главным продуктом для их получения служит каменноугольная смола, образующаяся в довольно значительном количестве при производстве светильного газа. В 1825 году английский исследователь Майкл Фарадей при термическом разложении ворвани выделил пахучее вещество, которое имело молекулярную формулу C6Н6. Это соединение, называемое теперь бензолом, является простейшим ароматическим углеводородом.
Бензол С6Н6 – родоначальник ароматических углеводородов.
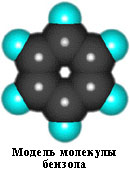
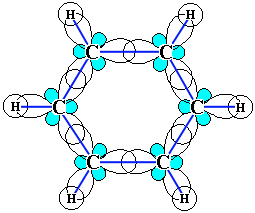
Все связи С-С в бензоле равноценны, их длина равна 0,140 нм, что соответствует промежуточному значению между длиной простой связи (0,154 нм) и двойной (0,134 нм). Это означает, что в молекуле бензола между углеродными атомами нет чисто простых и двойных связей (как в формуле, предложенной в 1865 г. немецким химиком Ф.Кекуле), а все они выровнены. Поэтому структурную формулу бензола изображают в виде правильного шестиугольника (s-скелет) и кружка внутри него, обозначающего делокализованные p-связи:
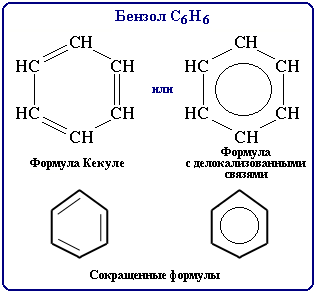
Формула Кекуле также нередко используется, но при этом учитывается, что она лишь условно передает строение молекулы.
Физические свойства. Бензол и его ближайшие гомологи – бесцветные жидкие вещества, нерастворимые в воде, но хорошо растворяющиеся во многих органических жидкостях. Легче воды. Огнеопасны. Бензол токсичен (вызывает заболевание крови – лейкемию).
Бензол даже в допустимых концентрациях разрушает клетки крови.

Бензол быстро вспыхивает и горит ярким, сильно коптящим пламенем.

Физические свойства аренов
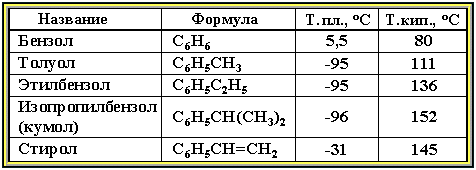
По химическим свойствам арены отличаются от предельных и непредельных углеводородов. Это объясняется особенностями строения бензольного кольца.
Арены не склонны вступать в реакции присоединения или окисления, которые ведут к нарушению ароматичности.
Для них наиболее характерны реакции, идущие с сохранением ароматической системы, а именно, реакции замещения атомов водорода, связанных с циклом.
Другие реакции (присоединение, окисление) идут с трудом.
Гомологи бензола (алкилбензолы) С6Н5–R более активно вступают в реакции замещения по сравнению с бензолом.
Например, при нитровании толуола С6Н5CH3 (70°С) происходит замещение не одного, а трех атомов водорода с образованием 2,4,6-тринитротолуола:

Алкилбензолы являются активной основы синтетических моющих средств, компрессорных масел и т.д.

Компрессорные масла VIRGINIA на основе алкилбензола.
В реакции присоединения, приводящие к разрушению ароматической структуры бензольного кольца, арены могут вступать с большим трудом.
Присоединение водорода к бензолу и его гомологам происходит при повышенной температуре и давлении в присутствии металлических катализаторов.
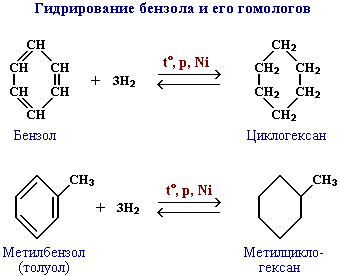
В условиях радикальных реакций (ультрафиолетовый свет, повышенная температура) возможно присоединение галогенов к ароматическим соединениям. Практическое значение имеет радикальное хлорирование бензола для получения "гексахлорана" (средство борьбы с вредными насекомыми).
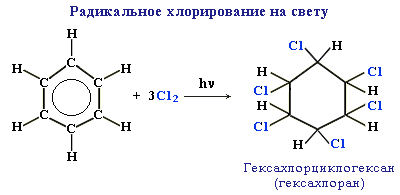

Гексахлоран является незаменимым для предохранения растений в парниках.
Бензол не окисляется даже под действием сильных окислителей
(KMnO4, K2Cr2O7 и т.п.). Поэтому он часто используется как инертный растворитель при проведении реакций окисления других органических соединений.
В отличие от бензола его гомологи окисляются довольно легко.
При действии раствора KMnO4 и нагревании в гомологах бензола окислению подвергаются только боковые цепи:
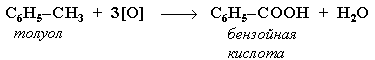
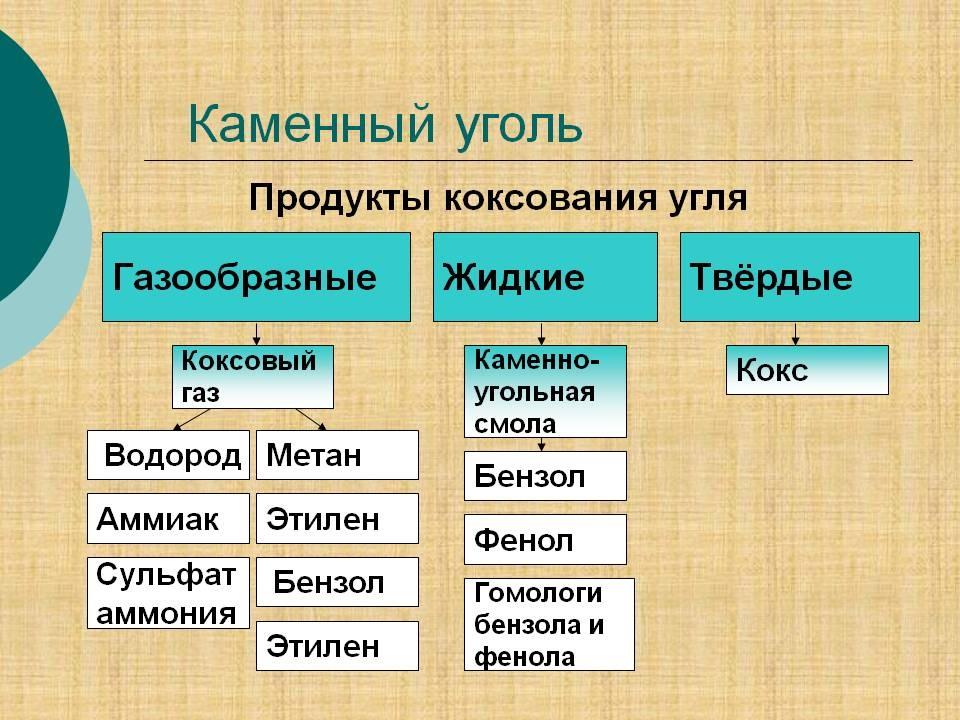
Основными природными источниками ароматических углеводородов являются каменный уголь и нефть.
При коксовании каменного угля образуется каменноугольная смола, из которой выделяют бензол, толуол, ксилолы, нафталин и многие другие органические соединения.
Ароматизация нефти:

а) дегидроциклизация (дегидрирование и циклизация) алканов в присутствии катализатора.
б) дегидрирование циклоалканов
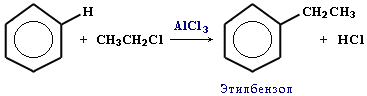
Алкилирование бензола галогеналканами или алкенами в присутствии безводного хлорида алюминия:
Тримеризация алкинов над активированным углем (реакция Зелинского).
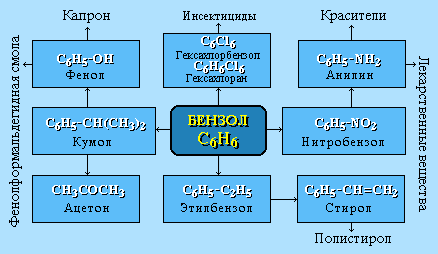
Бензол С6Н6 используется как исходный продукт для получения различных ароматических соединений – нитробензола, хлорбензола, анилина, фенола, стирола и т.д., применяемых в производстве лекарств, пластмасс, красителей, ядохимикатов и многих других органических веществ.

Толуол

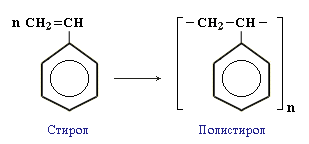

Стаканчик для йогурта из ударопрочного полистирола.