
АМИНЫ – класс соединений, представляющий собой органические производные аммиака, в котором один, два или три атома водорода замещены органическими группами. Отличительный признак – наличие фрагмента R–N
Классификация аминов
Классификация аминов разнообразна и определяется тем, какой признак строения взят за основу.
1.В зависимости от числа органических групп, связанных с атомом азота, различают:
Первичные амины – одна органическая группа у азота RNH2
Вторичные амины – две органических группы у азота R2NH, органические группы могут быть различными R'R"NH
третичные амины – три органических группы у азота R3N или R'R"R"'N
2.По типу органической группы, связанной с азотом, различают алифатические СH3– N6H5– N
3.По числу аминогрупп в молекуле амины делят на моноамины СH3 – NН2, диамины H2N(СH2)2NН2, триамины и т.д.
Номенклатура аминов
К названию органических групп, связанных с азотом, добавляют слово «амин», при этом группы упоминают в алфавитном порядке, например, СН3NHС3Н7 – метилпропиламин, СН3N(С6Н5)2 – метилдифениламин. Правила допускают также составлять название, взяв за основу углеводород, в котором аминогруппу рассматривают как заместитель. В таком случае ее положение указывают с помощью числового индекса: С5Н3С4Н2С3Н(NН2)С2Н2С1Н3 – 3-аминопентан (верхние числовые индексы синего цвета указывают порядок нумерации атомов С). Для некоторых аминов сохранились тривиальные (упрощенные) названия: С6Н5NH2 – анилин (название по правилам номенклатуры – фениламин).
В некоторых случаях применяют устоявшиеся названия, которые представляют собой искаженные правильные названия: Н2NСН2СН2ОН – моноэтаноламин (правильно – 2-аминоэтанол); (ОНСН2СН2)2NH – диэтаноламин, правильное название – бис(2-гидроксиэтил)амин.
Физические свойства аминов
Первые представители ряда аминов – метиламин CH3NH2, диметиламин (CH3)2NH, триметиламин (CH3)3N и этиламин C2H5NH2.
При комнатной температуре газообразные.
При увеличении числа атомов в R амины становятся жидкостями, а при увеличении длины цепи R до 10 атомов С – кристаллическими веществами.

Растворимость аминов в воде убывает по мере увеличения длины цепи R и при возрастании числа органических групп, связанных с азотом (переход к вторичным и третичным аминам).
Запах аминов напоминает запах аммиака, высшие (с большими R) амины практически лишены запаха.
Химические свойства аминов
1.Отличительная способность аминов – присоединять нейтральные молекулы , с образованием органоаммониевых солей, подобных аммонийным солям в неорганической химии. Для образования новой связи азот предоставляет неподеленную электронную пару, исполняя роль донора. Участвующий в образовании связи протон Н+ (от галогеноводорода) играет роль акцептора (приемника), такую связь называют донорно-акцепторной . Возникшая ковалентная связь N–H полностью эквивалентна имеющимся в амине связям N–H. (смотрите приложение 1)
2.Третичные амины также присоединяют HCl, но при нагревании полученной соли в растворе кислоты она распадается, при этом R отщепляется от атома N:
(C2H5)3N + HCl ® [(C2H5)5NH]Сl
[(C2H5)3NH]Сl ® (C2H5)2NH + C2H5Сl
При сравнении этих двух реакций видно, что C2H5-группа и Н, как бы меняются местами, в итоге из третичного амина образуется вторичный.
Растворяясь в воде, амины по такой же схеме захватывают протон, в результате в растворе появляются ионы ОН–, что соответствует образованию щелочной среды, ее можно обнаружить с помощью обычных индикаторов.
C2H5NH2 + H2O ® [C2H5NH3]+ + OH–
3.С образованием донорно-акцепторной связи амины могут присоединять не только HCl, но и галогеналкилы RCl, при этом образуется новая связь N–R, которая также эквивалентна уже имеющимся. Если в качестве исходного взять третичный амин, то получается соль тетраалкиламмония (четыре группы R у одного атома N):
(C2H5)3N + C2H5I ® [(C2H5)4N]I
Эти соли, растворяясь в воде и некоторых органических растворителях, диссоциируют (распадаются), образуя ионы:
[(C2H5)4N]I ® [(C2H5)4N]+ + I–
Такие растворы, как и все растворы, содержащие ионы, проводят электрический ток. В тетраалкиламмониевых солях можно заменить галоген НО-группой:
[(CH3)3N]Cl + AgOH ® [(CH3)4N]OH + AgCl
Получающийся гидроксид тетраметиламмония представляет собой сильное основание, по свойствам близкое к щелочам.
4.Первичные и вторичные амины взаимодействуют с азотистой кислотой HON=O, однако реагируют они различным образом. Из первичных аминов образуются первичные спирты:
C2H5NH2 + HNO2 ® C2H5OH + N2 +H2O
В отличие от первичных, вторичные амины образуют с азотистой кислотой желтые, трудно растворимые нитрозамины – соединения, содержащие фрагмент N–N = O:
(C2H5)2NH + HNO2 ® (C2H5)2N–N=O + H2O
Третичные амины при обычной температуре с азотистой кислотой не реагируют, таким образом, азотистая кислота является реагентом, позволяющим различить первичные, вторичные и третичные амины.
5.При конденсации аминов с карбоновыми кислотами образуются амиды кислот – соединения с фрагментом –С(О)N
Конденсация аминов с альдегидами и кетонами приводит к образованию так называемых оснований Шиффа – соединений, содержащих фрагмент –N=C
6.При взаимодействии первичных аминов с фосгеном Cl2С=O образуются соединения с группировкой –N=C=O, называемые изоцианатами .
Анилин
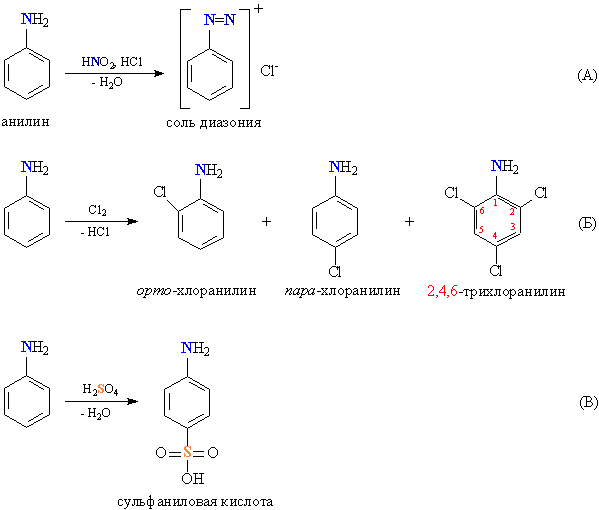
Среди ароматических аминов наиболее известен анилин (фениламин) С6Н5NH2. По свойствам он близок к алифатическим аминам, но его основность выражена слабее – в водных растворах он не образует щелочную среду. Как и алифатические амины, с сильными минеральными кислотами он может образовывать аммониевые соли [С6Н5NH3]+Сl–. При взаимодействии анилина с азотистой кислотой (в присутствии HCl) образуется диазосоединение, содержащее фрагмент R–N=N, оно получается в виде ионной соли, называемой солью диазония. Таким образом, взаимодействие с азотистой кислотой идет не так, как в случае алифатических аминов. Бензольное ядро в анилине обладает реакционной способностью, характерной для ароматических соединений , при галогенировании атомы водорода в орто- и пара-положениях к аминогруппе замещаются, получаются хлоранилины с различной степенью замещения . Действие серной кислоты приводит к сульфированию в пара-положение к аминогруппе, образуется так называемая сульфаниловая кислота .
Получение аминов

При взаимодействии аммиака с галогеналкилами, например RCl, образуется смесь первичных, вторичных и третичных аминов. Образующийся побочный продукт HCl присоединяется к аминам, образуя аммониевую соль, но при избытке аммиака соль разлагается, что позволяет проводить процесс вплоть до образования четвертичных аммониевых солей . В промышленности алифатические амины получают каталитическим взаимодействием спиртов с NH3 при 300–500° С и давлении 1–20 МПа, в результате получают смесь первичных, вторичных и третичных аминов.
При взаимодействии альдегидов и кетонов с аммонийной солью муравьиной кислоты HCOONH4 образуются первичные амины , а реакция альдегидов и кетонов с первичными аминами (в присутствии муравьиной кислоты НСООН) приводит к вторичным аминам .
Нитросоединения (содержащие группу –NO2) при восстановлении образуют первичные амины. Этот метод, предложенный Н.Н.Зининым, мало применяется для алифатических соединений, но важен для получения ароматических аминов и лег в основу промышленного производства анилина .
Как отдельные соединения амины применяются мало, например, в быту используется полиэтиленполиамин [-C2H4NH-]n (торговое название ПЭПА) как отвердитель эпоксидных смол. Основное применение аминов – как промежуточные продукты при получении различных органических веществ. Ведущая роль принадлежит анилину, на основе которого производится широкий спектр анилиновых красителей, причем цветовая «специализация» закладывается уже на стадии получения самого анилина.

Алифатические диамины – исходные соединения для получения полиамидов, например, нейлона , широко применяемого для изготовления волокон, полимерных пленок, а также узлов и деталей в машиностроении (полиамидные зубчатые передачи).

Из алифатических диизоцианатов получают полиуретаны, которые обладают комплексом технически важных свойств: высокой прочностью в сочетании с эластичностью и очень высоким сопротивлением истиранию (полиуретановые обувные подошвы), а также хорошей адгезией к широкому кругу материалов (полиуретановые клеи). Широко их применяют и во вспененной форме (пенополиуретаны).